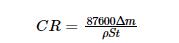摘要
采用電化學(xué)方法(電化學(xué)阻抗和動(dòng)電位極化)并配合浸泡失重法以及一系列表征,研究了常溫下碳鋼基體與CO2-Cl-的界面反應(yīng),以及加入HCO3-介質(zhì)后CO2-Cl--HCO3-體系中HCO3-介質(zhì)對碳鋼表面的成膜。結(jié)果表明,CO2介質(zhì)的加入使碳鋼基體的溶解速率顯著提高但是對Cl-濃度的影響較小;添加高濃度的Cl-反而抑制CO2的溶解而使基體的腐蝕速率略微降低;在CO2+Cl-+HCO3-體系中加入微量的HCO3-后碳鋼表面成膜不明顯,疏松的腐蝕產(chǎn)物不能抑制碳鋼基體的進(jìn)一步溶解;濃度過高的HCO3-使FeCO3的過飽和度提高從而加速細(xì)小晶體的析出,抑制腐蝕的進(jìn)行。
關(guān)鍵詞: 金屬材料 ; 多介質(zhì)協(xié)同作用 ; 電化學(xué)技術(shù) ; 腐蝕機(jī)理
本文引用格式
張少華, 李彥睿, 衛(wèi)英慧, 劉寶勝, 侯利鋒, 杜華云, 劉笑達(dá). 多介質(zhì)在碳鋼腐蝕過程中的協(xié)同作用. 材料研究學(xué)報(bào)[J], 2021, 35(10): 721-731 DOI:10.11901/1005.3093.2021.004
ZHANG Shaohua, LI Yanrui, WEI Yinghui, LIU Baosheng, HOU Lifeng, DU Huayun, LIU Xiaoda. Synergistic Effect of Multi-media on Carbon Steel Corrosion. Earth Science[J], 2021, 35(10): 721-731 DOI:10.11901/1005.3093.2021.004
輸送石油和天然氣的管線,是石油工業(yè)的“命脈”[1, 2]。集輸管線的腐蝕使其發(fā)生泄露式開裂而引起爆炸,可能造成重大安全事故和環(huán)境污染[3]。在油氣生產(chǎn)和運(yùn)輸?shù)墓芫€中,存在著油氣田中的CO2氣體和地層水[4, 5]。CO2溶解在地層水中生成的H2CO3,對碳鋼管線的腐蝕性極強(qiáng) [6, 7]。在管線流的不同區(qū)域,地層水中分布著不同濃度的Cl-離子[8]。文獻(xiàn)[9]研究了CO2與Cl-對油氣管線腐蝕的交互作用并解釋其機(jī)理,但是在工程條件下管線的腐蝕體系更為復(fù)雜。例如,NaHCO3作為一種pH值穩(wěn)定劑常注入管線流中以限制其均勻腐蝕速率。HCO3-即能促進(jìn)氧化膜的形成以增強(qiáng)碳鋼表面的鈍化[10, 11],還能發(fā)生兩步氧化反應(yīng)加速管線內(nèi)部減薄。因此,HCO3-的臨界濃度是控制腐蝕的關(guān)鍵[12]。
對于單一CO2、Cl-以及HCO3-介質(zhì)的腐蝕機(jī)理,已進(jìn)行了較多的研究。Linter、Burstein和Remita等[13, 14]研究了H2CO3的電化學(xué)活性、構(gòu)建數(shù)學(xué)模型預(yù)測CO2環(huán)境中的陰極反應(yīng),但是并未發(fā)現(xiàn)H2CO3在鋼表面的直接還原;關(guān)于CO2相關(guān)物質(zhì)能否直接作用于碳鋼陽極的溶解,學(xué)術(shù)界有不同的看法。Almedia等[15]認(rèn)為,CO2沒有直接作用在碳鋼的自由表面,感抗弧的出現(xiàn)源于Fe-H2O相關(guān)物質(zhì)的釋放;而Kahyarian等[16]根據(jù)陽極極化曲線的Tafel斜率從28 mV/dec降至22 mV/dec認(rèn)為,CO2相關(guān)物質(zhì)能直接作用于碳鋼陽極影響其溶解,關(guān)鍵是實(shí)驗(yàn)采用暫態(tài)技術(shù)還是穩(wěn)態(tài)Tafel技術(shù)。關(guān)于Cl-是否催化陽極溶解,前者提出Cl-能形成中間配合物使鐵基體溶解加速[17, 18];但是Barcia認(rèn)為,在Fe*(Ⅰ)ads和Fe(Ⅱ)ads結(jié)構(gòu)中Cl-與OH-相互競爭,當(dāng)體系的pH值不小于3時(shí)Cl-對鐵基體陽極溶解的影響較小[19]。關(guān)于HCO3-的研究,主要集中在陰極析氫反應(yīng)和陽極鈍化成膜反應(yīng):Mao等[20]發(fā)現(xiàn),在HCO3-的濃度為0.5 mol/L和1.0 mol/L極化曲線出現(xiàn)典型的陽極電流峰時(shí),碳鋼表面發(fā)生鈍化;而Zhang和Wright等[21, 22]則認(rèn)為,過高濃度的HCO3-將使陰極反應(yīng)加速。這些研究,加深了對碳鋼在單一CO2、Cl-及HCO3-介質(zhì)體系中腐蝕機(jī)理的解釋。本文采用電化學(xué)技術(shù)(電化學(xué)阻抗與動(dòng)電位極化)并配合浸泡失重法和一系列表征,研究油氣管線內(nèi)多介質(zhì)(CO2、Cl-、HCO3-)之間的協(xié)同作用對管線腐蝕的影響。
1 實(shí)驗(yàn)方法
1.1 樣品制備
實(shí)驗(yàn)用優(yōu)質(zhì)20碳素結(jié)構(gòu)鋼管線的化學(xué)成分,如表1所示。用于浸泡實(shí)驗(yàn)的試樣其尺寸為50 mm×10 mm×4 mm,用于電化學(xué)實(shí)驗(yàn)的試樣其尺寸為15 mm×15 mm×4 mm。實(shí)驗(yàn)前用丙酮將試樣除油,然后用SiC砂紙將其逐級打磨至2000#,用去離子水、無水乙醇依次清洗后用冷風(fēng)吹干,放在干燥皿中備用。將部分試樣拋光后用脫脂棉蘸取5%的硝酸酒精擦拭試樣表面1 min,用于觀察顯微組織(圖1所示),可見主要由鐵素體(區(qū)域A)和珠光體(區(qū)域B)組成。實(shí)驗(yàn)用腐蝕介質(zhì)可分為三個(gè)體系:(1)在N2脫氧條件下,只包含0.2/1.0 mol/L Cl-介質(zhì)的溶液體系;(2) 0.2/1.0 mol/L Cl-+飽和CO2溶液體系;(3) 0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-+飽和CO2溶液體系。
表1 實(shí)驗(yàn)用20碳鋼的化學(xué)成分
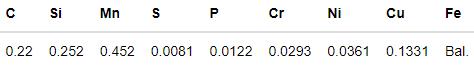

圖1 20碳鋼的顯微組織和區(qū)域A/B的EDS結(jié)果
1.2 浸泡測試
在容積為1 L的高溫高壓反應(yīng)釜中進(jìn)行浸泡實(shí)驗(yàn),其裝置如圖2所示。實(shí)驗(yàn)前,有精度為0.0001 g的分析天平將實(shí)驗(yàn)用試樣稱重,然后用游標(biāo)卡尺測定尺寸以計(jì)算其表面積。每次實(shí)驗(yàn)使用6個(gè)試樣,將其掛在反應(yīng)釜的特定位置后向反應(yīng)釜內(nèi)加入相應(yīng)體系的腐蝕介質(zhì)(0.6 L),使試樣在溶液中的高度相同。溶液相對試樣的流速為60轉(zhuǎn)/min。將反應(yīng)釜密封,對應(yīng)不同腐蝕體系通入相應(yīng)的氣體介質(zhì)。腐蝕浸泡實(shí)驗(yàn)達(dá)到預(yù)設(shè)的周期后迅速取出試樣,依次用去離子水和無水乙醇充分清洗后用冷風(fēng)烘干,放入干燥皿中待測。其中的3個(gè)試樣用于計(jì)算腐蝕速率,將其放入酸洗液(酸洗液的配制:500 mL ρ=1.19 g/mL鹽酸+3.5 g六次甲基四胺,加蒸餾水配制成1000 mL溶液,GB/T 16545-1996,China,idt ISO 8407,1991)中用超聲振動(dòng)3 min以去除其表面腐蝕產(chǎn)物[19],然后用去離子水和無水乙醇依次清洗后用冷風(fēng)吹干,用天平稱量并記錄數(shù)據(jù)。腐蝕速率為
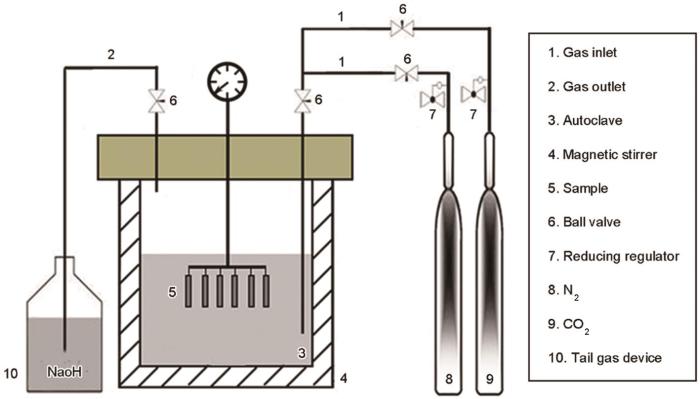
圖2 浸泡實(shí)驗(yàn)系統(tǒng)
其中Δm為樣品腐蝕后的質(zhì)量損失(g);ρ為材料的密度(g/cm3);S為試樣暴露在溶液中的面積(cm2);t為浸泡腐蝕時(shí)間(h)。其余的試樣用于表面形貌分析和成分檢測。
1.3 電化學(xué)阻抗測試和動(dòng)電位極化測試
電化學(xué)阻抗測試系統(tǒng)由Bio-logic SP-150電化學(xué)工作站、電化學(xué)反應(yīng)釜、標(biāo)準(zhǔn)的三電極體系以及配套設(shè)備組成。工作電極為20碳鋼試樣,參比電極為飽和甘汞電極,輔助電極為鉑電極。
試樣暴露在腐蝕介質(zhì)中的面積為1.0 cm2。在工作電極背面焊接導(dǎo)線,將工作面積外的部分用環(huán)氧樹脂封裝。實(shí)驗(yàn)前用SiC砂紙將試樣表面打磨,用無水乙醇將電極表面清洗后干燥。為了減小溶液的電阻,將工作電極與參比電極之間用魯金毛細(xì)管連接。每次開始測試電化學(xué)阻抗前,都需經(jīng)過大約2 h的開路電位測試以使體系達(dá)到相對穩(wěn)定狀態(tài)。測試頻率范圍為100 kHz~10 mHz,線性正弦擾動(dòng)為10 mV。測試結(jié)束后用ZSimDemo軟件擬合阻抗曲線的數(shù)據(jù)以得到所需參數(shù)。每組電化學(xué)實(shí)驗(yàn)都至少進(jìn)行5次,以確保實(shí)驗(yàn)的重復(fù)性。
動(dòng)電位極化測試使用與電化學(xué)阻抗測試相同的裝置。開路電位穩(wěn)定后進(jìn)行動(dòng)電位極化測試,掃描速率為0.5 mV/s。測試結(jié)束后將數(shù)據(jù)擬合以得到腐蝕電位Ecorr和電流密度Icorr等參數(shù)。
1.4 表面形貌的表征
用掃描電子顯微鏡(SEM)觀察腐蝕產(chǎn)物的表面和截面形貌,結(jié)合X射線衍射儀(XRD)和能譜分析儀(EDS)分析腐蝕產(chǎn)物的化學(xué)成分以確定腐蝕產(chǎn)物的組成。
2 結(jié)果和討論
2.1 動(dòng)電位極化曲線和電化學(xué)阻抗(CO2+Cl-體系)
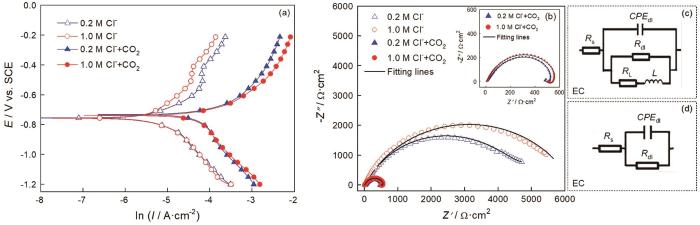
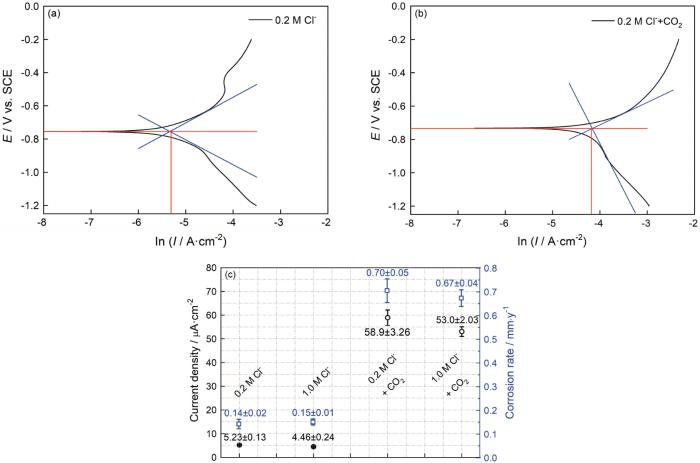
圖3給出了25℃下碳鋼在0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中的動(dòng)電位極化曲線和電化學(xué)阻抗譜。擬合具有代表性的動(dòng)電位極化曲線,如圖4a、b所示。結(jié)合電流密度值(圖4c)可以發(fā)現(xiàn),在只有Cl-介質(zhì)的溶液體系中,Cl-濃度的提高使陽極極化曲線的腐蝕電流輕微減小,而陰極極化曲線保持不變。其原因是,氯離子濃度過高使溶液的粘度提高,進(jìn)而使溶液內(nèi)的傳質(zhì)環(huán)節(jié)受到限制;加入CO2介質(zhì),使極化曲線整體向高電流密度方向顯著遷移。對于陰極部分,生成的H2CO3通過“buffering”效應(yīng)在金屬-電解質(zhì)界面逐步解離產(chǎn)生H+,使陰極析氫反應(yīng)顯著增強(qiáng);而陽極部分,CO2介質(zhì)的加入促進(jìn)Fe-H2O相關(guān)物質(zhì)的釋放,進(jìn)而使碳鋼基體的溶解加速[15]。
圖3 碳鋼在25℃的0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中的動(dòng)電位極化曲線、Nyquist圖和相應(yīng)的等效電路
圖4 碳鋼在Cl-和Cl-+CO2 (1 bar) 溶液體系中的動(dòng)電位極化曲線擬合結(jié)果以及相應(yīng)的腐蝕電流密度和腐蝕速率
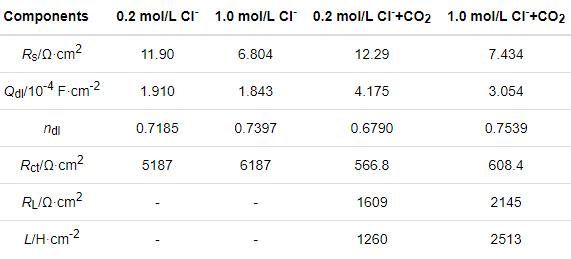
如圖3b所示,電化學(xué)阻抗譜圖具有與極化曲線相似的特征。分別用等效電路R(QR)和R(Q(R(RL)))擬合碳鋼在0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中的阻抗數(shù)據(jù),如圖3c、d所示。等效電路中的元件由溶液電阻Rs、金屬基體/電解質(zhì)之間的雙層容抗CPEdl、相位角常數(shù)ndl、電荷轉(zhuǎn)移電阻Rct以及感應(yīng)電阻RL和感抗L。所得的參數(shù)值列于表2。結(jié)合擬合結(jié)果發(fā)現(xiàn),在有不同濃度Cl-的飽和CO2溶液體系中,碳鋼的阻抗譜圖有兩個(gè)半圓,一個(gè)是與雙電容相關(guān)的高頻容抗弧,另一個(gè)是與Fe-H2O物質(zhì)釋放相關(guān)的低頻感抗弧。這表明,在飽和CO2溶液體系中,Cl-濃度的提高并沒有使碳鋼的界面反應(yīng)產(chǎn)生機(jī)理性轉(zhuǎn)變。Cl-濃度的提高使阻抗弧半徑稍有增大,因?yàn)檫^量的Cl-使溶解的CO2減少。但是,在只有Cl-介質(zhì)的溶液體系中,碳鋼的阻抗譜圖只有容抗弧。同時(shí),與有CO2-Cl-介質(zhì)的溶液體系比較,碳鋼在只有Cl-介質(zhì)的溶液體系中的阻抗半徑顯著增加。這表明,CO2介質(zhì)的加入使碳鋼的腐蝕機(jī)制發(fā)生了變化。
表2 碳鋼在0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中電化學(xué)阻抗譜的擬合參數(shù)
2.2 浸泡后的表面形貌(CO2+Cl-體系)
圖5給出了在25℃下碳鋼在0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中浸泡24 h后的表面形貌。腐蝕速率與腐蝕電流密度的變化趨勢一致,如圖4c所示。在只有Cl-介質(zhì)的溶液體系中碳鋼表面保持平整,只觀察到樣品制備過程中的劃痕;CO2介質(zhì)加入溶液體系后,碳鋼表面出現(xiàn)均勻腐蝕的形貌,生成了較薄的腐蝕層(EDS與XRD結(jié)果指出其主要成分為Fe3C,如圖5(e)/5(f)/5(g)所示)。考慮到碳鋼的微觀組織由鐵素體-珠光體組成,F(xiàn)e3C比鐵素體的腐蝕電位更正。因此,在鐵素體與Fe3C之間會(huì)形成一個(gè)電偶效應(yīng),鐵基體的選擇性溶解導(dǎo)致大量的Fe3C殘余[23, 24]。較高的陰極位點(diǎn)進(jìn)一步加速了碳鋼的腐蝕,使其腐蝕速率較高。
圖5 碳鋼在25℃的0.2/1.0 mol/L Cl-和0.2/1.0 mol/L Cl-+CO2(1 bar)溶液體系中浸泡24 h后的表面形貌以及EDS/XRD結(jié)果
2.3 動(dòng)電位極化曲線和電化學(xué)阻抗(CO2+Cl-+HCO3-體系)
針對HCO3-介質(zhì)的加入,探討CO2-Cl--HCO3-體系中三種介質(zhì)的協(xié)同作用。于HCO3-介質(zhì)的加入使碳鋼表面膜化效應(yīng)比較明顯,且溫度的提高有利于腐蝕產(chǎn)物的析出。因此,在60℃進(jìn)行實(shí)驗(yàn)以突出HCO3-介質(zhì)對碳鋼表面腐蝕產(chǎn)物膜層的作用。
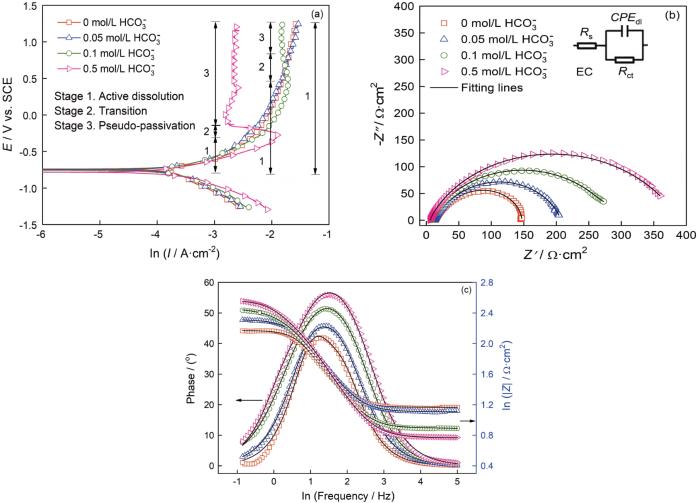
圖6a給出了在60℃碳鋼在CO2(1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中的動(dòng)電位極化曲線。首先,碳鋼在CO2(1 bar)+0.1 mol/L Cl-溶液體系中表現(xiàn)出活性溶解行為。添加0.05 mol/L HCO3-介質(zhì)后碳鋼的陽極極化曲線基本與前者重合,表明添加此濃度的HCO3-介質(zhì)并不能使碳鋼的腐蝕過程發(fā)生明顯的轉(zhuǎn)變。而HCO3-濃度達(dá)到0.1/0.5 mol/L時(shí),極化曲線發(fā)生顯著的變化。即隨著腐蝕電位的提高碳鋼在初始階段表現(xiàn)為活性溶解行為,然后發(fā)生“偽鈍化”。其原因是,鈍化電流密度還處于較高的電流密度區(qū)間,表明致密氧化膜層的形成,對碳鋼基體有較強(qiáng)的保護(hù)。其間,可觀察到一個(gè)明顯的活化-偽鈍化轉(zhuǎn)變區(qū)間(電流密度隨著電位的增加而急劇減小)。HCO3-的濃度達(dá)到0.5 mol/L時(shí)在-0.2 V vs. SCE以上的動(dòng)電位區(qū)間幾乎完全呈現(xiàn)出“偽鈍化”現(xiàn)象。擬合極化曲線得到相應(yīng)的參數(shù)值,如表3所示,即腐蝕電位(Ecorr)、“偽鈍化”電位(Epass)、腐蝕電流密度(Icorr)和陰/陽極極化曲線斜率(βa/βc)。可以看出,隨著HCO3-濃度的提高Ecorr值增加且Icorr值減小,腐蝕程度減弱。同時(shí),Epass值的降低(0.1~0.5 mol/L)表明其鈍化趨勢顯著增強(qiáng)。
圖6 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中的動(dòng)電位極化曲線和阻抗圖
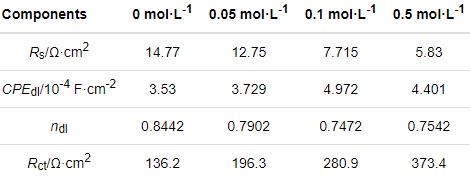
表3 碳鋼在CO2 (1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中所得動(dòng)電位極化曲線的擬合參數(shù)值
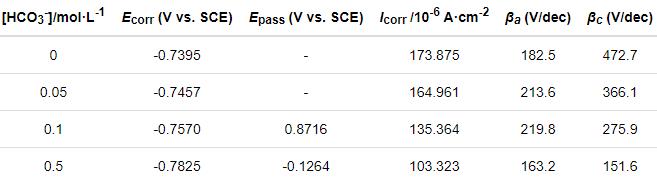
為了闡明碳鋼與CO2/HCO3-/Cl-介質(zhì)之間的界面反應(yīng),測試了電化學(xué)阻抗,如圖6b和6c所示。可以看出,Nyquist曲線由一個(gè)容抗組成,主要與碳鋼表面的電荷轉(zhuǎn)移電阻相關(guān)[25, 26]。用等效電路(R(QR))對EIS結(jié)果進(jìn)行了擬合,結(jié)果如表4所示。對應(yīng)0、0.05、0.1和0.5 mol/L HCO3-濃度下的chi-squared值分別為4.717×10-4、3.011×10-4、1.048×10-4和4.103×10-4,等效電路與實(shí)驗(yàn)數(shù)據(jù)的吻合程度較高。隨著HCO3-濃度的提高容抗弧的半徑略有增加,對應(yīng)的電荷轉(zhuǎn)移電阻Rct逐漸增大,可歸因于CO2(1 bar)+0.1 mol/L Cl-溶液體系中碳鋼表面的快速腐蝕;HCO3-釋放到溶液中,碳鋼表面吸附大量的HCO3-相關(guān)物質(zhì)使界面反應(yīng)受到抑制。同時(shí),相位角和低頻阻抗幅值|Z|(圖6c)的逐漸增大也證明,在CO2(1 bar)+0.1 mol/L Cl-+HCO3-溶液體系中碳鋼表面的耐蝕性提高。
表4 碳鋼在CO2(1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中的電化學(xué)阻抗譜擬合參數(shù)
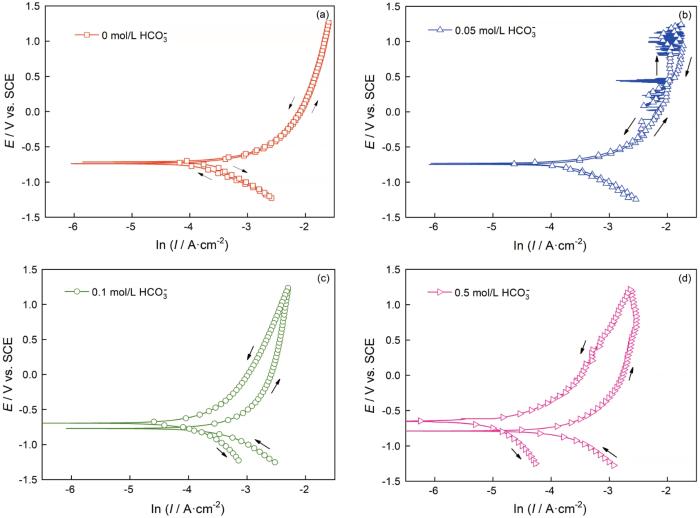
為了進(jìn)一步驗(yàn)證HCO3-介質(zhì)釋放到溶液體系中碳鋼表面的成膜效應(yīng),對CO2(1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中的碳鋼進(jìn)行循環(huán)伏安測試,如圖7所示。在CO2(1 bar)+0.1 mol/L Cl-溶液中碳鋼的正向與反向極化曲線完全重合,表明碳鋼表面基體維持裸露狀態(tài);0.05 mol/L HCO3-的加入使極化曲線的陽極部分出現(xiàn)較大的暫態(tài)電流,反映了碳鋼的表面狀態(tài)發(fā)生了不均勻的變化; 0.1/0.5 mol/L HCO3-介質(zhì)的加入,使其反向極化曲線向電流密度減小的方向移動(dòng)且腐蝕電位提高(尤其加入0.5 mol/L HCO3-介質(zhì)),表明在碳鋼表面形成了均勻致密的膜層。同時(shí),分析碳鋼在CO2 (1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中一次極化后的表面SEM形貌,如圖8所示。對于CO2(1 bar)+0.1 mol/LCl-溶液,碳鋼電極呈現(xiàn)Fe+Fe3C的腐蝕形貌,其原因是鐵素體的選擇性溶解。HCO3-介質(zhì)的濃度為0.05 mol/L時(shí)在碳鋼表面出現(xiàn)少量的腐蝕產(chǎn)物,隨HCO3-濃度提高到0.1/0.5 mol/L腐蝕產(chǎn)物均勻致密,覆蓋了整個(gè)碳鋼表面。這個(gè)結(jié)果,與圖7中的循環(huán)伏安曲線相符。結(jié)合圖8b中的面掃描圖和文獻(xiàn)[12, 27, 28],腐蝕產(chǎn)物的成分為γ-Fe2O3。其原因是,在電極極化條件下FeCO3的穩(wěn)定性較差,隨著電位的提高腐蝕產(chǎn)物以γ-Fe2O3的形式存在。
圖7 碳鋼在60℃的CO2(1 bar)+0.1 mol/L Cl-+0、0.05、0.1和0.5 mol/L HCO3-溶液體系中的循環(huán)伏安曲線
圖8 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0、0.05、0.1和0.5 mol/L HCO3-溶液體系中極化到1.25 V vs. SCE的SEM形貌
2.4 浸泡后表面和橫截面的形貌(CO2+Cl-+ HCO3-體系)
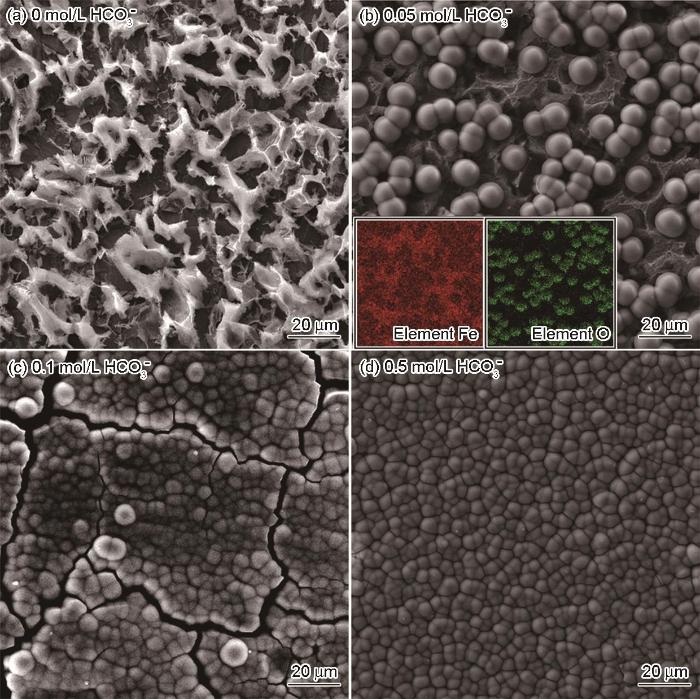
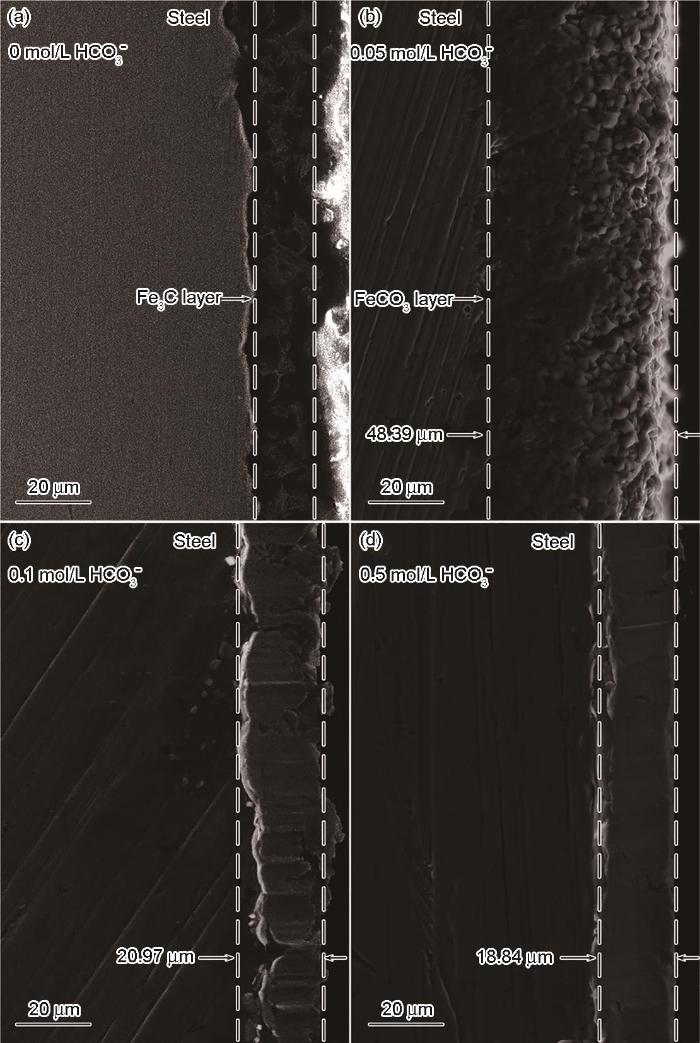
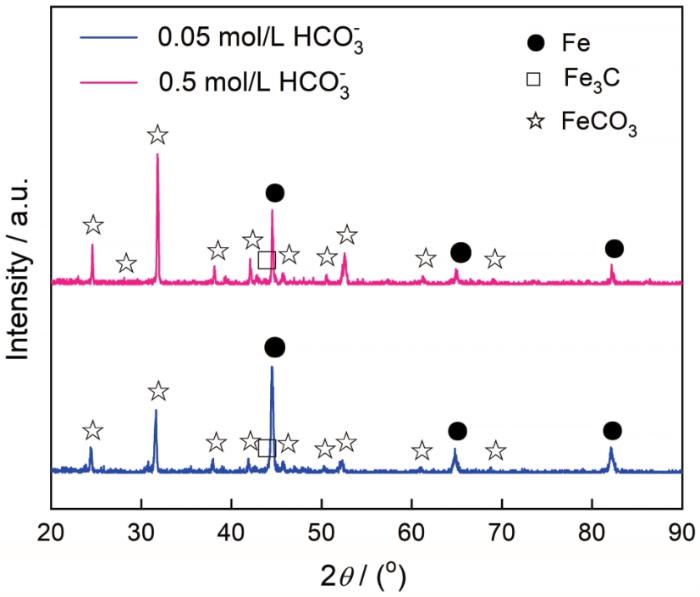
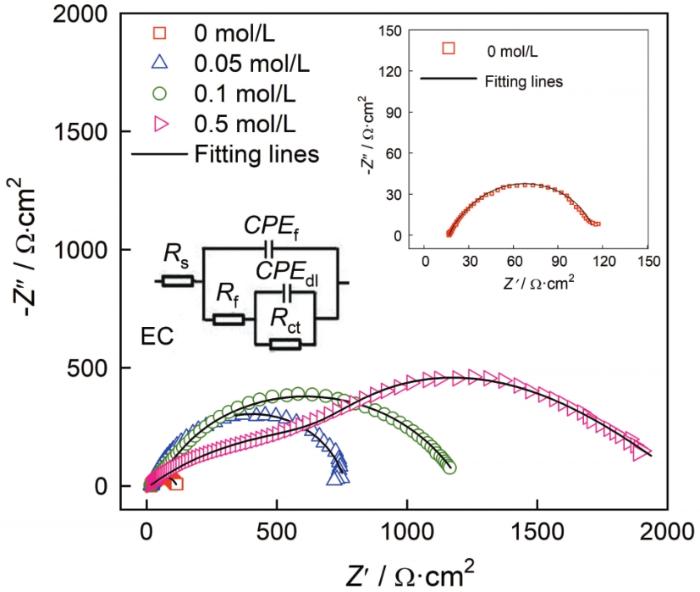
圖9和圖10分別給出了碳鋼在60℃的CCO2(1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中浸泡24 h后的表面和橫截面SEM形貌。圖11給出了碳鋼在CO2+Cl-+0.05/0.5 mol/L HCO3-體系浸泡24 h后表面腐蝕產(chǎn)物的XRD譜。與電化學(xué)結(jié)果對應(yīng),在CO2 (1 bar)+0.1 mol/L Cl-溶液中(圖9a和圖10a)并沒有觀察到腐蝕產(chǎn)物,在碳鋼的界面處生成了一層殘余的Fe3C;HCO3-濃度達(dá)到0.05 mol/L時(shí)在碳鋼表面生成了疏松且尺寸較大的FeCO3腐蝕產(chǎn)物,晶粒尺寸大約為8 μm(圖9b)。截面形貌表明,疏松的腐蝕產(chǎn)物不能抑制腐蝕的進(jìn)一步發(fā)生,因此腐蝕產(chǎn)物層的厚度達(dá)到了48.39 μm (圖10b)。疏松的腐蝕產(chǎn)物可能使碳鋼基體局部暴露在溶液中而加速碳鋼的局部腐蝕,使碳鋼局部失效的可能性提高。HCO3-濃度達(dá)到0.1/0.5 mol/L時(shí)FeCO3晶體尺寸變得更加細(xì)小,約3 μm (0.1 mol/L HCO3-)和1 μm(0.5 mol/L HCO3-),如圖9(c/d)所示。腐蝕產(chǎn)物的橫截面也呈現(xiàn)出非常致密的特征,厚度分別減小至20.97 μm(圖10c)和18.84 μm(圖10d)。且在XRD圖譜中,隨著HCO3-濃度的提高對應(yīng)于Fe的峰強(qiáng)度降低,而對應(yīng)于FeCO3的峰強(qiáng)度顯著增強(qiáng); HCO3-的濃度為0.5 mol/L時(shí)FeCO3的峰強(qiáng)度明顯高于Fe基體,表明碳鋼表面的FeCO3晶體的析出動(dòng)力學(xué)加速,幾乎覆蓋了整個(gè)表面。致密的腐蝕產(chǎn)物在碳鋼基體與腐蝕介質(zhì)之間形成一個(gè)屏障,能有效地抑制腐蝕的進(jìn)一步進(jìn)行。另一方面,HCO3-的加入提高了溶液的pH值,顯著降低了FeCO3晶體析出所需的Fe2+濃度,其相對過飽和度明顯提高。同時(shí),晶體的形核率隨著相對過飽和度呈指數(shù)相關(guān),而晶體長大速率隨著相過相對飽和度呈線性相關(guān)。因此,隨著HCO3-濃度的提高FeCO3晶體的形核主導(dǎo)了整個(gè)過程,在碳鋼表面呈現(xiàn)出更加細(xì)小的FeCO3晶體形貌。為了進(jìn)一步驗(yàn)證腐蝕產(chǎn)物的保護(hù)性,對覆蓋有腐蝕產(chǎn)物的碳鋼表面在CO2(1 bar)+0.1 mol/L Cl-溶液中進(jìn)行EIS測試,如圖12所示。同時(shí),用電化學(xué)等效電路擬合EIS結(jié)果,加入膜層容抗CPEf、相位角常數(shù)nf和膜層電阻Rf。加入0.05 mol/L的HCO3-介質(zhì)后其Nyquist圖呈現(xiàn)出單一的容抗,在此條件下碳鋼表面形成的腐蝕產(chǎn)物保護(hù)性較弱,以電荷轉(zhuǎn)移電阻為主要控制環(huán)節(jié);隨著HCO3-濃度的提高(0.1~0.5 mol/L)出現(xiàn)兩個(gè)容抗且半徑變大,Rct和Rf值明顯增加,表明腐蝕產(chǎn)物的耐腐蝕能力增強(qiáng)。這表明,碳鋼表面的膜層已較為致密,界面反應(yīng)控制環(huán)節(jié)主要由電荷轉(zhuǎn)移電阻和膜層電阻組成。
圖9 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0、0.05、0.1和0.5 mol/L HCO3-溶液體系中浸泡24 h后的表面SEM照片
圖10 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0、0.05、0.1和0.5 mol/L HCO3-溶液體系中浸泡24 h后的橫截面SEM照片
圖11 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0.05/0.5 mol/L HCO3-溶液體系中浸泡24 h后腐蝕產(chǎn)物的XRD譜
圖12 碳鋼在60℃的CO2 (1 bar)+0.1 mol/L Cl-+0/0.05/0.1/0.5 mol/L HCO3-溶液體系中浸泡24 h后的Nyquist曲線
3 結(jié)論
(1) 加入CO2介質(zhì)使碳鋼基體的腐蝕溶解速率顯著提高而對Cl-濃度的影響較小,添加高濃度的Cl-能抑制CO2的溶解而使基體的腐蝕速率略微降低。
(2) 在CO2+Cl-+HCO3-體系中加入微量的HCO3-后碳鋼表面成膜不明顯,疏松的腐蝕產(chǎn)物不能抑制碳鋼基體的進(jìn)一步溶解;而濃度過高的HCO3-使FeCO3的過飽和度提高、加速細(xì)小晶體的析出和抑制腐蝕。
參考文獻(xiàn)
1 Zhao J H, Wang X Q, Kang J, et al. Crack propagation behavior during DWTT for X80 pipeline steel processed via ultra-fast cooling technique [J]. Chin. J. Mater. Res., 2017, 31(10): 728
1 趙金華, 王學(xué)強(qiáng), 康 健等. 超快冷工藝下X80管線鋼的DWTT裂紋擴(kuò)展行為 [J]. 材料研究學(xué)報(bào), 2017, 31(10): 728
2 Han X, Yu S, Li H, et al. Preparation and Properties of CuO Superhydrophobic Coating on X90 Pipeline Steel [J]. Chin. J. Mater. Res., 2017, 31(9): 672
2 韓祥祥, 于思榮, 李好等. X90管線鋼表面CuO超疏水涂層的制備和性能 [J]. 材料研究學(xué)報(bào), 2017, 31(9): 672
3 Sun J, Zhang G, Liu W, et al. The formation mechanism of corrosion scale and electrochemical characteristic of low alloy steel in carbon dioxide-saturated solution [J]. Corros. Sci., 2012, 57: 131
4 Zhang G A, Lu M X, Wu Y S. Morphology and microstructure of CO2 corrosion scales [J]. Chin. J. Mater. Res., 2005, 19(5): 537
4 張國安, 路民旭, 吳蔭順. CO2腐蝕產(chǎn)物膜的微觀形貌和結(jié)構(gòu)特征 [J]. 材料研究學(xué)報(bào), 2005, 19(5): 537
5 Ne?i? S. Key issues related to modelling of internal corrosion of oil and gas pipelines-A review [J]. Corros. Sci., 2007, 49(12): 4308
6 Nesic S, Postlethwaite J, Olsen S. An electrochemical model for prediction of corrosion of mild steel in aqueous carbon dioxide solutions [J]. Corrosion, 1996, 52(4): 280
7 Zhu J Y, Tan C T, Bao F H, et al. CO2 corrosion behaviour of a novel Al-containing low Cr steel in a simulated oilfield formation water [J]. Chin. J. Mater. Res., 2020, 34(6): 443
7 朱金陽, 譚成通, 暴飛虎等. 一種新型含Al低Cr合金鋼在模擬油田采出液環(huán)境下的CO2腐蝕行為 [J]. 材料研究學(xué)報(bào), 2020, 34(6): 443
8 Han J, Ne?i? S, Yang Y. Spontaneous passivation observations during scale formation on mild steel in CO2 brines [J]. Electrochim. Acta, 2011, 56(15): 5396
9 Zhang S, Hou L, Du H, et al. A study on the interaction between chloride ions and CO2 towards carbonsteel corrosion [J]. Corros. Sci., 2020, 167: 108531
10 Xu L, Xiao H, Shang W, et al. Passivation of X65 (UNS K03014) carbon steel in NaHCO3 solution in a CO2 environment [J]. Corros. Sci., 2016, 109: 246
11 Liu Z, Gao X, Li J, et al. Corrosion behaviour of low-alloy martensite steel exposed to vapour-saturated CO2 and CO2-saturated brine conditions [J]. Electrochim. Acta, 2016, 213: 842
12 Barker R, Burkle D, Charpentier T, et al. A review of iron carbonate (FeCO3) formation in the oil and gas industry [J]. Corros. Sci., 2018, 142: 312
13 Linter B R, Burstein G T. Reactions of pipeline steels in carbon dioxide solutions [J]. Corros. Sci., 1999, 41(1): 117
14 Remita E, Tribollet B, Sutter E, et al. Hydrogen evolution in aqueous solutions containing dissolved CO2: quantitative contribution of the buffering effect [J]. Corros. Sci., 2008, 50(5): 1433
15 Almeida T D C, Bandeira M C E, Moreira R M. New insights on the role of CO2 in the mechanism of carbon steel corrosion [J]. Corros. Sci., 2017, 120: 239
16 Kahyarian A, Brown B, Nesic S. Electrochemistry of CO2 corrosion of mild steel: Effect of CO2 on iron dissolution reaction [J]. Corros. Sci., 2017, 129: 146
17 Ashley G W, Burstein G T. Initial stages of the anodic oxidation of iron in chloride solutions [J]. Corrosion, 1991, 47(12): 908
18 Darwish N A, Hilbert F, Lorenz W J, et al. The influence of chloride ions on the kinetics of iron dissolution [J]. Electrochim. Acta, 1973, 18(6): 421
19 Barcia O E, Mattos O R. The role of chloride and sulphate anions in the iron dissolution mechanism studied by impedance measurements [J]. Electrochim. Acta, 1990, 35(6): 1003
20 Mao X, Liu X, Revie R W. Pitting corrosion of pipeline steel in dilute bicarbonate solution with chloride ions [J]. Corrosion, 1994, 50(9): 651
21 Zhang G, Lu M, Chai C, et al. Effect of HCO3- concentration on CO2 corrosion in oil and gas fields [J]. Int. J. Min. Met. Mater., 2006, 13(1): 44
22 Wright R F, Brand E R, Ziomek-Moroz M, et al. Effect of HCO3- on electrochemical kinetics of carbon steel corrosion in CO2-saturated brines [J]. Electrochim. Acta, 2018, 290: 626
23 Onyejia L, Mohammed S, Kale G. Electrochemical response of micro-alloyed steel under potentiostatic polarization in CO2 saturated brine [J]. Corros. Sci., 2018, 138: 146
24 Popoola L T, Grema A S, Latinwo G K, et al. Corrosion problems during oil and gas production and its mitigation [J]. Int. J. Ind. Chem., 2013, 4(1): 35
25 Heuer J K, Stubbins J F. An XPS characteristic of FeCO3 films from CO2 corrosion [J]. Corros. Sci., 1999, 41(7): 1231
26 Zhang D L, Wei E Z, Jing H, et al. Construction of super-hydrophobic structure on surface of super ferritic stainless steel B44660 and its corrosion resistance [J]. Chin. J. Mater. Res., 2021, 35(1): 7
26 張大磊, 魏恩澤, 荊赫等. 超級鐵素體不銹鋼表面超疏水結(jié)構(gòu)的制備及其耐腐蝕性能 [J]. 材料研究學(xué)報(bào), 2021, 35(1): 7
27 Davies D H, Burstein G T. The effect of bicarbonate on the corrosion and passivation of iron [J]. Corrosion, 1980, 36(8): 416
28 Kermani M B, Morshed A. Carbon dioxide corrosion in oil and gas production-A compendium [J]. Corrosion, 2003, 59(8): 659
免責(zé)聲明:本網(wǎng)站所轉(zhuǎn)載的文字、圖片與視頻資料版權(quán)歸原創(chuàng)作者所有,如果涉及侵權(quán),請第一時(shí)間聯(lián)系本網(wǎng)刪除。
-
標(biāo)簽: 金屬材料, 多介質(zhì)協(xié)同作用, 電化學(xué)技術(shù), 腐蝕機(jī)理

官方微信
《腐蝕與防護(hù)網(wǎng)電子期刊》征訂啟事
- 投稿聯(lián)系:編輯部
- 電話:010-62316606
- 郵箱:fsfhzy666@163.com
- 腐蝕與防護(hù)網(wǎng)官方QQ群:140808414